Weltweit konkurrieren Länder um internationale klinische Studien, nicht nur, weil die pharmazeutische Forschung und Entwicklung einen wichtigen Wirtschaftsfaktor darstellt, sondern auch, um Patientinnen und Patienten einen früheren Zugang zu innovativen Therapien zu ermöglichen. Dabei haben im internationalen Vergleich die EU und innerhalb der EU Deutschland an Boden verloren. Andererseits haben die Regierungen die strategische Bedeutung der Pharmaindustrie, die angesichts der internationalen wirtschaftlichen und politische Volatilität noch zunimmt, erkannt und ergreifen Maßnahmen.
Europa gerät bei klinischen Studien ins Hintertreffen
Absolut und relativ wurden in Europa 2023 weniger Studien initiiert als noch vor zehn Jahre. 2013 waren es 2.424 neue Studien, 2023 nur noch 1.978, obwohl weltweit mehr Studien gestartet wurden. Der europäische Anteil sank damit von 27% auf 16%.
Anzahl neuer klinischer Studien weltweit nach Region (2013, 2018-2023; Phase 1-4)1
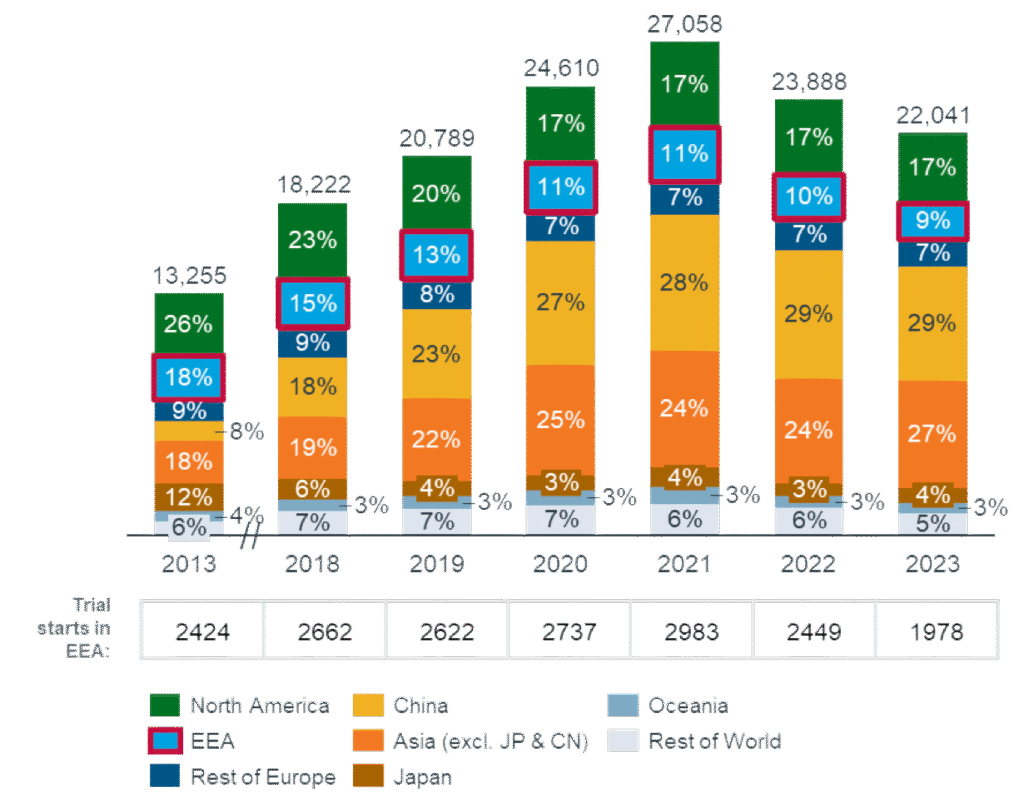
–
Auch innerhalb Europas hat sich die Gewichtung verschoben. Neuer Spitzenreiter ist Spanien, wogegen Deutschland einen deutlichen Rückgang an Studien zu verzeichen hat. Dieser ist zum Teil auf langwierige Vertragsverhandlungen und eine langsame Patientenrekrutierung zurückzuführen, die durch strenge Datenschutzgesetze beeinträchtigt wird. Dagegen hat Spanien seit 2016 gezielte Maßnahmen ergriffen, um für Studien attraktiver zu werden, darunter einheitliche Ethikabstimmungen und Mustervertragsklauseln, was zur Stabilität der Studientätigkeit geführt hat.
Anzahl neuer kommerzieller klinischer Studien im EWR 2018 und 2023, Top 10 Länder
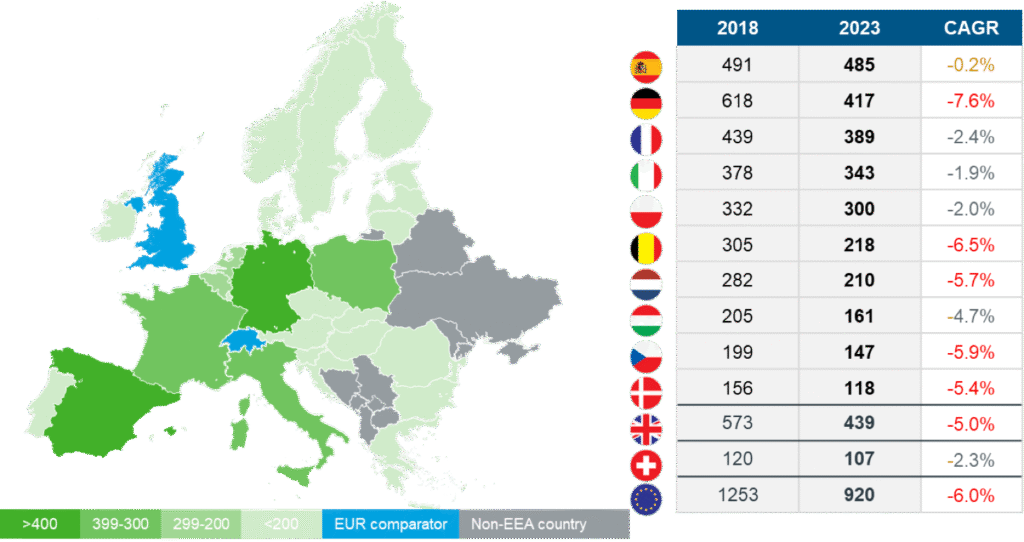
–
Anlaufzeiten als Schlüsselfaktor für die Wettbewerbsfähigkeit
Im Wettbewerb um klinische Studien werden die Anlaufzeiten zunehmend als Schlüsselfaktor für die Attraktivität eines Landes als Standort erkannt. Dies gilt insbesondere für europäische Länder, in denen die regulatorische Landschaft mit dem vollständigen Inkrafttreten der Verordnung über klinische Prüfungen (EU 536/2014) harmonisiert wurde, so dass die Anlaufzeiten eines der wenigen Differenzierungsmerkmale darstellen. Um diese zu verkürzen, führen immer mehr Länder einheitliche Vorlagen für die Verträge für klinische Studien und teilweise auch für die Budgetierung und Kostenkalkulation ein. So unterstreicht auch der Bericht der Europäischen Kommission über die Wettbewerbsfähigkeit von 2024 die Notwendigkeit einer rationalisierten Verwaltung von Mehrländerstudien und empfiehlt die Annahme von Musterverträgen.
In Deutschland wurde als Teil der nationalen Pharmastrategie vom Dezember 2023 im September 2024 das Arzneimittelforschungsgesetz verabschiedet mit dem Ziel, die Forschungslandschaft in Deutschland zu verbessern. Zu den vorgeschlagenen Maßnahmen gehören Standardvertragsklauseln, die verbindlich werden sollen, um die Verhandlungs- und Anlaufzeiten zu verkürzen. Bereits im Vorfeld dieses Gesetzes wurden von Interessengruppen aus den Reihen der pharmazeutischen Industrie und den Forschungseinrichtungen, darunter auch IQVIA, Mustervertragsklauseln entwickelt.
Auf Basis von > 15.000 verhandelten Verträgen im Vereinigten Königreich, Irland, Frankreich, Spanien, Italien, Belgien, den Niederlanden und Dänemark hat IQVIA den Einfluss von Mustervertragsklauseln und Vertragsvorlagen auf die Anlaufzeiten klinischer Studien bewertet. Dabei zeigte sich, dass verpflichtende nationale Vertragsvorlagen zu deutlich kürzeren Zykluszeiten führen: In Ländern wie Frankreich, das 2014 verbindliche Vertragsvorlagen und eine harmonisierte Budgetierung eingeführt hat, konnten die Zykluszeiten um über 40 % verkürzt werden. Ähnliche positive Auswirkungen wurden in Irland und in geringerem Maße in Italien und Spanien beobachtet.
Optionale Vertragsvorlagen dagegen zeigen gemischte Ergebnisse: Länder mit fakultativen Vertragsvorlagen, wie Belgien, die Niederlande und Dänemark, weisen unterschiedliche Annahmeraten und weniger einheitliche Verkürzungen der Durchlaufzeiten auf. Es zeigt sich aber, dass Verträge, die die Vorlagen nutzen, tendenziell schneller verhandelt werden als solche ohne.
Vertragsvorlagen und Mustervertragsklauseln stoßen in Deutschland auf hohe Akzeptanz: laut einer Umfrage von IQVIA Deutschland bei führenden Studienzentren befürwortet die überwiegende Mehrzahl die Nutzung solcher Vorlagen: 77% stehen einer vollständigen oder teilweisen Nutzung offen gegenüber. Von denjenigen Prüfzentren, die derzeit die Vorlagen noch nicht nutzen, sind 80% bereit, ihre Haltung innerhalb der nächsten sechs Monate zu überprüfen. Neben kürzeren Anlaufzeiten erwarten die Prüfzentren auch einen deutlich geringeren Ressourceneinsatz im Vorfeld von Studien durch effizientere Verhandlungenprozesse.
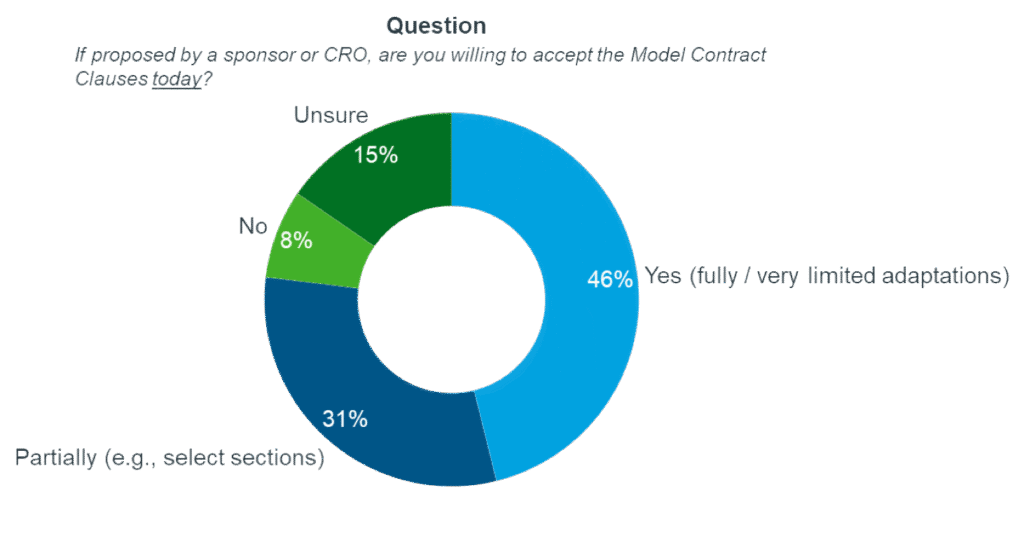
Die Umsetzung steht noch aus
Um die Konkurrenzfähigkeit Europas im Wettbewerb um klinische Studien zu erhöhen, ist größere Effizienz in der Vorbereitungs- und Anlaufphase gefragt. Vertragsvorlagen und standardisierte Budgetierungsprozesse sind vielversprechende Ansatzpunkte, die auch von Prüfungszentren, CROs, und der Industrie unterstützt. Jetzt ist es an den gesundheitspolitischen Entscheidungsträgern, die Umsetzung anzugehen.
Das vollständige White Paper zum Thema steht hier bereit: Competing on contracting efficiency
1Assessing the clinical trial ecosystem in Europe. EFPIA and Vaccines Europe, October 2024. https://www.efpia.eu/media/0ipkatpg/efpia-ct-report-embargoed-221024-final.pdf